- Հեղինակ Jason Gerald gerald@how-what-advice.com.
- Public 2023-12-16 11:18.
- Վերջին փոփոխված 2025-01-23 12:20.
Նոսրացումը կենտրոնացված լուծույթն ավելի նոսրացնելու գործընթացն է: Կան մի շարք պատճառներ, թե ինչու ինչ -որ մեկը կարող է ցանկանալ նոսրացնել ՝ սկսած լուրջից մինչև պարզ պատճառներ: Օրինակ, կենսաքիմիկոսները նոսրացնում են լուծույթներն իրենց կենտրոնացված ձևերից ՝ փորձարկումների համար նոր լուծումներ պատրաստելու համար, մինչդեռ, մյուս կողմից, բարմենները հաճախ լիկյորը նոսրացնում են զովացուցիչ ըմպելիքներով կամ հյութերով ՝ կոկտեյլներն ավելի համեղ դարձնելու համար: Նոսրացման հաշվարկման ընդհանուր բանաձևն է Գ1Վ1 = Գ2Վ2, Գ1 եւ Գ2 ներկայացնում է համապատասխանաբար լուծույթի սկզբնական և վերջնական կոնցենտրացիաները և Վ1 եւ Վ2 ներկայացնում է ծավալը:
Քայլ
Մեթոդ 1 -ից 2 -ը. Խտանյութերի ճշգրիտ նոսրացում `նոսրացման հավասարման միջոցով

Քայլ 1. Որոշեք, թե ինչ գիտեք և չգիտեք:
Քիմիայի մեջ նոսրացումը սովորաբար նշանակում է վերցնել մի փոքր քանակությամբ լուծույթ, որի կոնցենտրացիան գիտեք, այնուհետ ավելացնել չեզոք հեղուկ (օրինակ ՝ ջուր) ՝ ավելի մեծ ծավալով, բայց ավելի փոքր կոնցենտրացիայով նոր լուծույթ պատրաստելու համար: Դա շատ հաճախ կատարվում է քիմիայի լաբորատորիաներում, քանի որ արդյունավետության համար ռեագենտները հաճախ պահվում են շատ բարձր կոնցենտրացիաներում, որոնք այնուհետև նոսրացվում են փորձերի մեջ օգտագործելու համար: Սովորաբար, իրական իրավիճակների մեծ մասում դուք կիմանաք ձեր սկզբնական լուծույթի կոնցենտրացիան և այն կոնցենտրացիան կամ ծավալը, որը ցանկանում եք ունենալ ձեր վերջնական կոնցենտրացիան, բայց ոչ սկզբնական լուծույթի ծավալը, որն անհրաժեշտ է վերջնական լուծումը ստանալու համար:
- Այնուամենայնիվ, այլ իրավիճակներում (հատկապես դպրոցական խնդիրների դեպքում), գուցե անհրաժեշտ լինի գտնել գլուխկոտրուկի այլ կտորներ, օրինակ ՝ ձեզ կարող են տրվել սկզբնական ծավալ և համակենտրոնացում, այնուհետև խնդրել գտնել լուծման լուծարման դեպքում վերջնական կոնցենտրացիան: մինչև ցանկալի ծավալը: Նոսրացման ցանկացած դեպքում օգտակար է սկսել սկսելուց առաջ նշել հայտնի և անհայտ փոփոխականները:
-
Ավարտենք հարցերի օրինակը: Ենթադրենք, մեզանից պահանջվում է 5 Մ լուծույթը ջրով նոսրացնել, որպեսզի ստացվի 1 Լ 1 լուծույթ մՄ. Այս դեպքում մենք գիտենք մեր սկզբնական լուծույթի կոնցենտրացիան և մեր ուզած ծավալը և վերջնական կոնցենտրացիան, բայց ոչ սկզբնական լուծույթի այն քանակությունը, որը մենք պետք է ավելացնենք ջրով `ցանկալի արդյունքի հասնելու համար:
Հիշեցում. Քիմիայում M- ը Molarity կոչվող կոնցենտրացիայի չափումն է, որը նշանակում է մեկ լիտր նյութի մոլ:
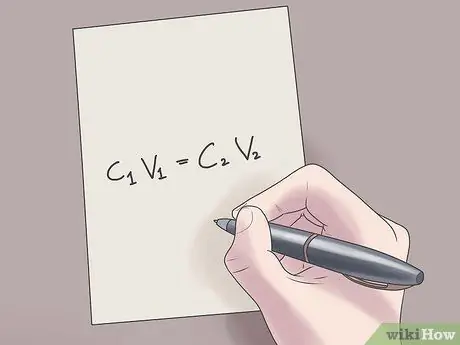
Քայլ 2. Միացրեք ձեր արժեքները C բանաձևին1Վ1 = Գ2Վ2.
Այս բանաձևում Գ1 լուծույթի սկզբնական կոնցենտրացիան է, Վ1 սկզբնական լուծույթի ծավալն է, C2 լուծույթի վերջնական կոնցենտրացիան է, իսկ Վ2 վերջնական լուծույթի ծավալն է: Այս հավասարման մեջ միացնելով հայտնի արժեքները կօգնեն ձեզ գտնել ավելի քիչ դժվարությամբ անհայտ արժեքներ:
- Կարող է օգտակար լինել հարցական նշանը դնել այն միավորի առջև, որը ցանկանում եք որոնել, որը կօգնի ձեզ լուծել այն:
-
Շարունակենք մեր օրինակը: Մենք մուտքագրելու ենք մեզ հայտնի արժեքները հետևյալ կերպ.
- Գ1Վ1 = Գ2Վ2
- (5 Մ) Վ1 = (1 մմ) (1 լ): Մեր երկու կենտրոնացումներն ունեն տարբեր միավորներ: Եկեք այստեղ կանգ առնենք և անցնենք հաջորդ քայլին:

Քայլ 3. Հաշվի առեք միավորների ցանկացած տարբերություն:
Քանի որ լուծումները ներառում են համակենտրոնացման փոփոխություններ (որոնք երբեմն կարող են լինել բավականին մեծ), ձեր հավասարման երկու փոփոխականների համար անսովոր չէ ունենալ տարբեր միավորներ: Թեև դա հեշտ է անտեսել, ձեր հավասարման անհավասար միավորները կարող են ձեր պատասխանի սխալ լինել: Ավարտելուց առաջ փոխակերպեք բոլոր արժեքները տարբեր համակենտրոնացման և/կամ ծավալային միավորներով:
-
Մեր օրինակում մենք օգտագործում ենք տարբեր միավորներ M (molars) և mM (millimolars) կոնցենտրացիաների համար: Եկեք մեր երկրորդ չափումը փոխենք M- ի:
- 1 մմ × 1 Մ/1000 մմ
- = 0,001 Մ

Քայլ 4. Ավարտեք:
Երբ բոլոր միավորները հավասար են, լուծիր քո հավասարումը: Դա գրեթե միշտ կարելի է անել պարզ հանրահաշվով:
-
Մենք դադարեցնում ենք մեր օրինակի խնդիրը այստեղ ՝ (5 Մ) V1 = (1 մմ) (1 լ): Եկեք գտնենք V- ի արժեքը1 մեր նոր միավորով:
- (5 Մ) Վ1 = (0.001 Մ) (1 Լ)
- Վ1 = (0,001 Մ) (1 Լ)/(5 Մ):
-
Վ1 = 0.0002 Լ, կամ 0.2 մլ:

Քայլ 5. Հասկացեք, թե ինչպես ճիշտ օգտագործել ձեր պատասխանը:
Ենթադրենք, դուք գտել եք ձեր բաց թողնված արժեքը, բայց վստահ չեք, թե ինչպես օգտագործել այս նոր տեղեկատվությունը անհրաժեշտ իրական նոսրացման մեջ: Սա հասկանալի է. Մաթեմատիկայի և գիտության լեզուն երբեմն չի համապատասխանում իրական աշխարհին: Երբ գիտես C հավասարման չորս արժեքները1Վ1 = Գ2Վ2, նոսրացումը կատարեք հետևյալ կերպ.
- Չափել ծավալը V1 C- ի կոնցենտրացիայով լուծույթից1. Այնուհետև ավելացրեք բավականաչափ լուծիչ (ջուր և այլն), որպեսզի ընդհանուր ծավալը կազմվի V2. Այս նոր լուծումը կունենա ձեր ուզած կոնցենտրացիան (Գ2).
- Մեր օրինակում, օրինակ, մենք սկզբում չափում ենք 5 Մ լուծույթի 0.2 մլ: Հաջորդը, մենք այնքան ջուր կավելացնենք, որ լուծույթի ծավալը հասցվի 1 Լ -ի: 1 Լ - 0.0002 Լ = 0.9998 Լ, կամ 999, 8 մլ:. Այլ կերպ ասած, մենք մեր փոքր նմուշային լուծույթին կավելացնենք 999.8 մլ ջուր: Մեր նոր, նոսրացված լուծույթը ունի 1 մՄ կոնցենտրացիա, որը մեր ցանկալի կոնցենտրացիան է:
Մեթոդ 2 -ից 2 -ը. Պարզ և գործնական լուծման լուծում պատրաստելը

Քայլ 1. Տեղեկությունների համար կարդացեք ցանկացած փաթեթավորում:
Կան մի շարք պատճառներ, թե ինչու դուք կցանկանայիք պատրաստել նոսրացման լուծույթ տանը, խոհանոցում կամ մեկ այլ ոչ քիմիական լաբորատորիայում: Օրինակ, պարզ խտանյութից նարնջի հյութ պատրաստելը նոսրացում է: Շատ դեպքերում, այն արտադրանքը, որը պետք է նոսրացվի, պարունակում է տեղեկատվություն այն նոսրացման մասին, որը պետք է արվի ՝ ինչ -որ տեղ փաթեթավորման վրա: Նրանք կարող են ունենալ ճշգրիտ հրահանգներ, որոնց պետք է հետևեն: Ահա որոշ բաներ, որոնք պետք է փնտրել տեղեկատվություն փնտրելիս.
- Օգտագործված արտադրանքի ծավալը
- Օգտագործված նոսրացնողի ծավալը
- Օգտագործված լուծիչի տեսակը (սովորաբար ջուր)
- Խառնուրդի հատուկ հրահանգներ
- Դուք կարող եք չտեսնել օգտագործված հեղուկի ճշգրիտ կոնցենտրացիայի մասին տեղեկատվությունը: Այս տեղեկատվությունը օգտակար չէ միջին սպառողի համար:

Քայլ 2. Խտացրած լուծույթին ավելացրեք այն նյութը, որը որպես լուծիչ է գործում:
Կենցաղային պարզ նոսրացումների համար, ինչպես այն, ինչ դուք կարող եք պատրաստել խոհանոցում, իրոք, միայն սկսելուց առաջ պետք է իմանալ օգտագործվող խտանյութի ծավալը և ցանկալի մոտավոր վերջնական կոնցենտրացիան: Խտանյութը նոսրացրեք համապատասխան քանակությամբ լուծիչով, որը որոշվում է ՝ կախված օգտագործվող սկզբնական խտանյութի ծավալից: Տես ներքեւում:
- Օրինակ, եթե մենք ցանկանայինք 1 բաժակ նարնջի հյութի խտանյութը նոսրացնել մինչև իր սկզբնական կոնցենտրացիայի 1/4 -ը, կավելացնեինք 3 բաժակ ջուր խտանյութի մեջ: Մեր վերջնական խառնուրդը կունենա 1 բաժակ խտանյութ 4 բաժակ ամբողջական հեղուկի մեջ `իր սկզբնական կոնցենտրացիայի 1/4 -ը:
- Ահա ավելի բարդ օրինակ. Եթե մենք ցանկանայինք 2/3 բաժակ խտանյութը նոսրացնել մինչև դրա սկզբնական կոնցենտրացիայի 1/4, մենք կավելացնեինք 2 բաժակ ջուր, քանի որ 2/3 բաժակը հավասար է 1/4 անգամ 2 և 2/3 բաժակ ամբողջական հեղուկ:
- Համոզվեք, որ ձեր նյութը ավելացնում եք բավականաչափ մեծ տարայի մեջ, որպեսզի կարողանաք պահել ձեր ուզած վերջնական ծավալը ՝ մեծ աման կամ նմանատիպ տարա:

Քայլ 3. Շատ դեպքերում անտեսեք փոշու ծավալը:
Փոշի (օրինակ ՝ խմիչքների որոշակի խառնուրդներ) հեղուկին ավելացնելը սովորաբար չի համարվում նոսրացում: Փոքր քանակությամբ փոշու հեղուկին ավելացման արդյունքում առաջացած ծավալի փոփոխությունը սովորաբար այնքան փոքր է, որ աննշան է: Այլ կերպ ասած, հեղուկին փոքր քանակությամբ փոշի ավելացնելիս պարզապես փոշին ավելացրեք հեղուկի ցանկալի վերջնական ծավալին և խառնեք:
Գուշացում
- Հետևեք անվտանգության ցանկացած ցուցում, որը տրամադրվում է արտադրողի կողմից կամ պահանջվում է ձեր ընկերության կողմից: Սա հատկապես կարևոր է, եթե դուք պետք է նոսրացնեք թթվային լուծույթը:
- Թթվային լուծույթների հետ աշխատանքը կարող է պահանջել ավելի մանրամասն անվտանգության միջոցներ և ուղեցույցներ, քան ոչ թթվային լուծույթների դեպքում:






